深圳欣博盛生物科技有限公司品牌商
16 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
- 查看全部分类
- 欣博盛ELISA 试剂盒
- Vectorlabs
- GeneTex
- Peprotech
- Invivogen
- BioXcell
- FuGENE
- Prozyme
- Cayman
- Mirusbio
- ENZO(Alexis, Biomol, Assaydesign&stressgen)
- AbD Serotec
- Surmodics
- Millipore
- Metasystems
- Mabtech
- Proimmune
- Adipogen
- Bioporto
- Southern Biotech (SBA)
- Everest Biotech
- Chondrex
- IQ Products
- Atlas
- Detroit R&D
- StressMarq
- Cell Biolabs
- StrigoLab
- Synaptic Systems
- BioInnovatise
- Cosmo Bio
- Abwiz Bio
- Gerbu
- 蛋白
- 试剂类
- 抗体
- 分子化合物
- Cargille
- Antagen
- Nanoprobes
- Funakoshi
- Demeditec
- Enzo
- Fitzgerald
- Biovendor
- ICL
- Matreya
- PhaRNA
- Funakoshi
- Promise Advanced Proteomics
- Bioassay works
- NSJ Bio
- Aldevron
- CalBioreagents
- 3Helix
- 自产试剂盒
- TriLink
- Virostat
- Agilent
- Epicypher
- Jackson ImmunoResearch
推荐产品
公司新闻/正文
星形胶质细胞在帕金森病中的作用
102 人阅读发布时间:2026-03-03 12:02

星形胶质细胞在帕金森病中的作用:
帕金森病是一种进行性神经退行性疾病,其特征是多巴胺生成神经元的丧失,以及大脑中 α-突触核蛋白的积累。错误折叠的 α-突触核蛋白聚集被认为会通过一种称为星形胶质细胞的非神经胶质细胞触发慢性炎症。
星形胶质细胞对于神经元功能至关重要,因为它们通过执行许多重要的支持功能来维持中枢神经系统的稳态。这些功能包括调节离子和水分水平,维持血脑屏障,清除废物,并以糖原形式储存能量。
反应性星形胶质细胞:双刃剑
在反应性星形胶质增生过程中,病理性刺激会导致星形胶质细胞从静息状态转变为活跃状态。根据刺激的性质,星形胶质细胞的反应状态可能是:
• A1 型:神经毒性,常见于帕金森病患者死后脑组织
• A2 型:神经保护性,通常与缺血性损伤相关
理解星形胶质细胞如何转变为有害的炎症状态,对于揭示帕金森病的新治疗策略至关重要。
最-新研究:UCL、Crick与KAIST合作
在伦敦大学学院(UCL)、Francis Crick 研究所和韩国科学技术院(KAIST)最近的一项合作研究中,D’Sa 等人探讨了星形胶质细胞对 α-突触核蛋白的反应。该研究发表在《Science Advances》上。研究人员从六位健康供体的诱导多能干细胞(hiPSC)中生成了皮层星形胶质细胞和神经元。对星形胶质细胞培养物的检测结果确认了细胞类型准确且具备功能成熟度。这确保了后续的炎症刺激能够在一个与人体生理高度相关的模型中进行评估。
随后,研究人员测试了 α-突触核蛋白寡聚体(α-syn-O)的细胞反应,这些寡聚体由单体在实验室内聚集而成。测试在三种体外培养体系中进行:
• 仅含星形胶质细胞
• 仅含神经元
• 星形胶质细胞与神经元混合培养
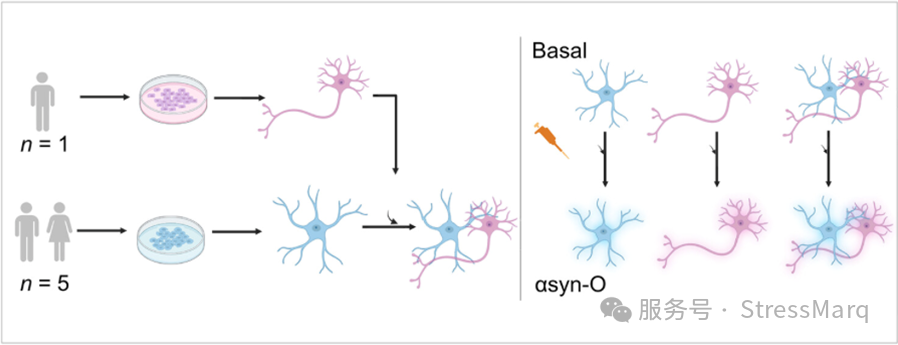
图1. [图片来自 D’Sa 等人] 从五位健康供体的 hiPSC(人诱导多能干细胞)中生成了星形胶质细胞(蓝色),并从第六位健康供体中生成了皮层神经元(粉色)。D’Sa 等人比较了在仅含星形胶质细胞、仅含神经元以及星形胶质细胞与神经元混合培养体系中,细胞对 α-syn-O 的反应。
单细胞测序揭示星形胶质细胞亚型
研究人员在三种培养体系上使用单细胞 RNA 测序,分析在有或没有 α-syn-O 处理情况下的基因差异。结果识别出八个细胞簇,其中两个是星形胶质细胞簇(AC1 和 AC2),六个是神经元簇。
AC1:过度表达细胞因子和免疫通路基因,呈炎症性特征
AC2:富含形态发生和神经营养因子,呈保护性特征
比较结果提示,人类星形胶质细胞可以呈现预设的、分化的反应状态,类似于体内经典的 A1 神经毒性和 A2 神经保护性表型。
研究人员观察到外源性 α-突触核蛋白在星形胶质细胞、神经元及共培养体系中的内吞情况。通过 FRET 生物传感器检测,结果显示星形胶质细胞摄取单体的水平高于神经元,但两种细胞类型中寡聚体形成水平相似。
值得注意的是,该研究团队此前的一项研究发现,α-突触核蛋白寡聚体(alpha synuclein-O)处理原代星形胶质细胞会引发炎症反应。为了在 hiPSC 星形胶质细胞模型中诱导这一机制,研究人员同样使用 α-突触核蛋白寡聚体处理细胞。结果显示,寡聚体处理导致星形胶质细胞内活性氧(ROS)过度生成,之后研究人员通过二氢乙啶(dihydroethidium)氧化进行测定。由于 ROS 过表达引起的细胞死亡程度较低,提示炎症反应已被诱导。该实验步骤也进一步确认,hiPSC 来源的星形胶质细胞能够精准再现原生细胞中观察到的关键生物应激反应。
StressMarq 的 α-突触核蛋白单体(SPR-321)和 β-突触核蛋白单体(SPR-405)在当前模型中进行了测试,结果显示它们能够诱导细胞因子释放。与培养基对照组相比,α-突触核蛋白寡聚体处理 hiPSC 来源的星形胶质细胞显著促进了促炎性细胞因子的分泌,包括 TNF-α、IL-6、IL-8、IL-1β 和 IFN-γ。进一步通过整体 RNA 测序结合形态学分析,研究人员观察到星形胶质细胞在寡聚体暴露后发生细胞骨架重塑及 GFAP 极化。
这些结果共同揭示了病理性 α-突触核蛋白在驱动星形胶质细胞向炎症效应细胞转化中的关键作用。后续 RNA 测序还显示,细胞呈现出类抗病毒反应,与细胞因子水平的显著升高相一致。这一现象提示,固有免疫通路,尤其是与病毒识别相关的信号机制,可能在该过程中被激活。
在共培养体系中,α-syn-O 处理条件下导致的炎症反应和神经损伤程度显著高于单独星形胶质细胞培养。共培养体系分泌更高浓度的细胞因子,并在两种细胞类型中产生活性氧,同时伴随更高水平的细胞死亡和神经元放电受损。分析显示,星形胶质细胞向炎症性亚型 AC1 转变,直接削弱神经元的抵抗力。
在寡聚体处理后,星形胶质细胞及共培养体系中 ADAR1 表达显著增加。该酶在双链 RNA 中将腺苷(A)转化为肌苷(I)。在干扰素敏感启动子的控制下,ADAR 转录本从核内 p110 转变为胞质型 p150,这可能是一种反馈机制,用于限制过度抗病毒信号并维持 RNA 稳态,同时增强神经炎症期间的 RNA 编辑活性。
研究发现,含星形胶质细胞的样本在 3′ UTR 和编码区表现出编辑位点数量增加和编辑率升高,提示 RNA 编辑可能增强炎症级联反应。对帕金森病患者死后脑组织的分析显示,整体 A-to-I RNA 编辑水平显著升高,且最显著的富集出现在星形胶质细胞特异性转录本中,将这一机制与疾病病理联系起来。
本研究成功构建了一个人源 iPSC 模型,生成星形胶质细胞和类神经元细胞,用于探究 α-突触核蛋白对人脑的影响。研究揭示,寡聚 α-突触核蛋白处理会刺激 ROS 过度生成和炎症性细胞因子释放,星形胶质细胞表现出类似抗病毒的反应,并上调 ADAR1,导致 RNA 编辑增加,促进慢性神经炎症。
与这些发现一致,研究人员还在帕金森病患者死后脑样本中观察到 A-to-I 编辑水平升高。这项研究为揭示帕金森病相关的神经退行性机制提供了关键见解,并提示 ADAR1 上调和增强的 RNA 编辑可能是推动神经炎症的重要因素。
作为全球领-先的神经退行性疾病研究工具供应商,StressMarq 提供优化的 α-突触核蛋白、Tau 蛋白和 β-淀粉样蛋白的单体、寡聚体及纤维状构建物,包括用于帕金森病和阿尔茨海默病研究的 γ-突触核蛋白单体(SPR-407)。访问我们的产品引用页面,了解更多关于 StressMarq 产品如何推动神经退行性疾病研究的信息。
更多详情请联系StressMarq 中国总代理╌欣博盛生物






